Присуждение нобелевской премии по медицине в 2018 году вызвало ожидаемый всплеск интереса к иммунотерапии рака со стороны падкой на сенсации прессы. Российские журналисты тут же окрестили метод новым и прогрессивным, а люди со злокачественными новообразованиями ухватились за очередную надежду на излечение и получили стимул для поиска материальных средств: к сожалению, стоимость курса терапии иммунопрепаратами пока не укладывается в бюджет онкологических отделений отечественных государственных клиник.
На этот вид лечения конкретному больному выделяется не более 180 000 рублей, тогда как одно только лекарство стоит порядка 300 000 рублей. Однако если речь идет о здоровье и, уж, тем более, о жизни, то материальная сторона всегда отходит на второй план. Поэтому для некоторых найти недостающую сумму – вполне выполнимая задача.
Гораздо больше людей, которые больны раком и которых лечат другими методами, волнует другой вопрос: почему мне не назначают иммунотерапию? У нас в стране нет таких лекарств, на них не хватает денег, наши врачи не умеют лечить по-новому? На самом деле, все не так просто и не все так однозначно. Вот что говорят о нашумевших методах онкоиммунотерапии авторитетные российские специалисты:
- Научным открытиям нобелевских лауреатов Тасуку Хондзё (Япония) и Джеймса Эллисона (США) уже более 20 лет. Первый корректор противоракового иммунитета нового поколения – ипилимумаб – появился в арсенале практикующих врачей почти 10 лет назад. Следовательно, методы не так новы, не так универсальны и, к сожалению, пока не столь эффективны, как того хотелось бы. Иначе рак был бы давно и окончательно побежден.
- У российских иммунотерапевтов есть необходимые знания и лекарства. В настоящее время в РФ зарегистрировано несколько иммунопрепаратов нового поколения, тем или иным образом способствующих активизации ослабленного естественного противоракового иммунитета. В их числе – Ервой, Тецентрик, Китруда, Опдиво и некоторые другие. Эти лекарства в достаточном количестве закупаются как государственными, так и частными онкоцентрами. Наши врачи знают, как, кому и когда их можно и нужно назначать.
- Иммунотерапия помогает далеко не всем. Даже тогда, когда, теоретически, может помочь.

Тем не менее, ведущие онкологи нашей страны убеждены: решение шведских экспертов из Королевского Каролинского медико-хирургического института Стокгольма более чем оправдано. Открытия японского и американского ученых стали настоящим прорывом, и премию они получили заслуженно.
Восстановление естественной защиты вместо постепенного разрушения организма ядами
Биологические методы лечения в целом и онкоиммунотерапия в частности рано или поздно должны позволить онкологам полностью отказаться от агрессивной неспецифической химиотерапии. Необходимость такого отказа очевидна:
- При химиолечении по традиционным схемам, первые из которых были разработаны еще в середине прошлого столетия, в организм попадают высокотоксичные яды.
- Эти яды затрагивают не только опухоль, но и здоровые структуры с быстро делящимися клетками: костный мозг, волосяные фолликулы, ткани печени и почек в период регенерации и др. Поэтому онкологи образно называют традиционную химиотерапию «стрельбой из пушки по воробьям».
- Благодаря усилиям врачей и грамотно выстроенным схемам, пораженные токсичными цитостатиками органы после окончания химиолечения постепенно восстанавливаются. Однако разрушительное действие «химии» на организм человека все-таки не проходит бесследно, и каждый последующий курс ХТ при рецидивах и метастазировании переносится тяжелее предыдущего.
Иммуноонкологи используют принципиально иной подход к борьбе с раком. Они стремятся дать возможность организму справиться с заболеванием естественным путем. То есть так, как это происходит в организме здоровых людей, где правильно работающий врожденный противораковый иммунитет безошибочно распознает появляющиеся злокачественные клетки и уничтожает их.
Решая эту задачу, нобелевские лауреаты в области медицины 2018 года много лет назад занялись поиском причин нарушения нормальной работы иммунитета. Что именно удалось обнаружить каждому из них?
Белок PD-L1 «маскирует» клетки опухоли под нормальные, «дезинформируя» иммунитет
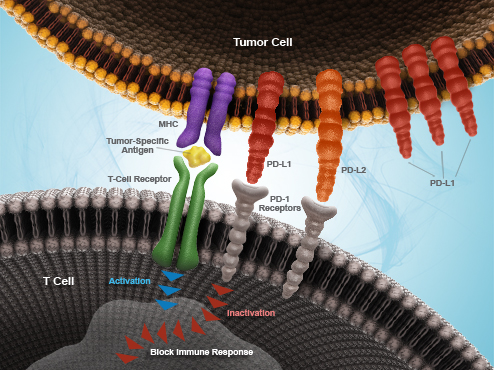
В конце 90-х годов прошлого столетия японский иммунолог Тасуку Хондзё и его коллеги определили, что некоторые опухолевые клетки производят большое количество особого белка, получившего название PD-L1. Молекулы этого белка скапливаются на их поверхности и связываются с рецепторами PD-1 на поверхности Т-лимфоцитов, «предъявляя» последним злокачественную клетку в качестве нормальной. В результате «обманутый» лимфоцит не только не атакует клетку рака, но и начинает неправильно функционировать, постепенно теряя свои свойства и разрушаясь.
Белковый комплекс CTLA-4 «запрещает» иммунным клеткам работать
Американский иммунолог, профессор онкоцентра им. Андерссона Техасского университета Джеймс Эллисон открыл и описал еще один способ защиты опухоли от Т-клеток. Оказывается, некоторые новообразования способны провоцировать появление на поверхности Т-лимфоцитов ингибиторных комплексов CTLA-4. Такой комплекс становится своеобразным «табу», запрещающим клеткам иммунной системы «вступать в поединок» с раком.
Из исследовательских лабораторий – в клиническую практику
Открытия Хондзё и Эллисона позволили создать два вида препаратов. Одни из них, такие как ниволумаб (Опдиво) и пембролизумаб (Китруда), блокируют белки PD-L1 на поверхности раковой клетки, связываясь с ними и не позволяя «обмануть» Т-лимфоциты. Другие, такие как ипилимумаб (Ервой) и его аналоги, снимают блокировку с Т-лимфоцитов и активируют их.
Несмотря на разный механизм действия, препараты обеих групп решают одну и ту же задачу: пытаются возвратить естественному иммунитету утраченную или сниженную способность обезоруживать и устранять раковые клетки.
Именно это отличает современную иммунотерапию от лечения иммуностимулирующими препаратами предыдущего поколения. Последние «подстегивали» иммунную систему, заставляя ее работать на износ или пытаясь взять на себя ее функции. Это приводило к истощению иммунитета и появлению многочисленных осложнений, включая опасные для жизни состояния. В то же время раковые опухоли продолжали умело защищаться от «врагов», используя те или иные механизмы – лечение практически не давало каких-либо положительных результатов.
Сегодня биофармацевты всего мира работают над созданием целенаправленно действующих препаратов, практически не влияющих на здоровые клетки и приводящих к гибели раковых клеток – тем или иным способом. Такие лекарства и методы называю таргетными. Часть из таргетных противоопухолевых препаратов относятся к иммуномодуляторам, в том числе и тем, механизм действия которых основан на открытиях нобелевских лауреатов.
Пока препараты данной группы назначают не более чем 5 процентам пациентов – с меланомой, определенными типами рака легких, почки, желудка, головы и шеи. Наилучшие результаты достигаются при лечении больных, у которых злокачественные мутации появились вследствие действия канцерогенных факторов: например, рак легких у курильщика или меланома у женщины, регулярно посещавшей солярий. Какую роль иммунотерапевтические методы, принесшие своим разработчикам мировую славу и большие деньги, будут играть в дальнейшем – покажет время.
Что изменилось в иммуноонкологии после открытий Хондзё и Эллисона
Открытия японского и американского исследователей позволили врачам понять, как именно работает противораковый иммунитет, что ему мешает, и почему не работают старые методы иммунотерапии. Результаты их исследований стали важнейшей вехой в истории формирования новых подходов к онкоиммунотерапии.
Включение в схемы лечения пациентов таких препаратов, как Ервой, Китруда, Опдиво и др., цвеличивает шансы на то, что человек с последней стадией заболевания проживет пять и более лет, с 2-5% до 30-40%. Однако речь о стопроцентном выходе в длительную ремиссию и полном излечении больных с терминальной стадией рака не идет.
Хорошие результаты отмечены при назначении иммунокорректоров на более ранних этапах болезни. Так, например, иммунотерапия успешно проводится больным с 3 стадией меланомы после операции для предупреждения метастазирования. Но и в этом случае не приходится говорить о методе, как о панацее.
На более ранних стадиях к иммунотерапии прибегают редко. Но не потому, что онкологи и производители традиционных синтетических ядов-цитостатиков «вступили в сговор» и боятся потерять миллионные барыши. Ну, или, по крайней мере, не только поэтому.
Все дело в том, что лекарства, возвращающие иммунитету способность бороться с раком, не безобидны, хотя и неядовиты. Наиболее частые и наименее тяжелые побочные эффекты – потеря аппетита, тошнота, сыпь, зуд, кашель, усталость.
Реже возникают более серьезные осложнения – диарея, воспаление кишечника, легких и др. Такие нарушения приходится устранять медикаментозными методами, их сложно корректировать, и, главное, при появлении подобных расстройств лечение иммунопрепаратами приходится прекратить. Необходимо также добавить, что при онокоиммунотерапии по некоторым протоколам серьезные побочные эффекты наблюдаются в 50% случаев.
Точно установить, почему появляются те или иные осложнения, ученые смогут лишь тогда, когда будут досконально изучены все механизмы и компоненты противоракового иммунитета и все способы защиты рака. Пока же есть ответы только на отдельные вопросы. Так, например, обнаружено, что в некоторых случаях после «разблокировки» Т-лимфоцитов с ингибирующими комплексами CTLA-4 иммунная система начинает убивать не только раковые клетки, но и клетки здоровых тканей, приводя к появлению вышеперечисленных проблем. Отчего это происходит, пока до конца непонятно.
Новые направления онкоиммунотерапии: отстройка иммунитета без осложнений
Исследования в области иммунотерапии рака не ограничиваются описанными выше открытиями, и наука не стоит месте. Ученые выдвигают новые гипотезы и создают лекарства и парафармацевтики для бережной и эффективной помощи естественному противораковому иммунитету. Одни из них пока находятся в стадии разработки. Другие, такие, как например, экстракт омелы и Биобран (MGN-3), успешно используются в схемах вспомогательного лечения.
Наиболее интересным представляется включение в схемы комплементарной терапии Биобрана, отличающегося быстрым, мощным и, одновременно, мягким действием. Один из главных аргументов в пользу MGN-3: за все время клинических испытаний и практического применения препарата не было выявлено ни одного побочного эффекта. Более того, назначение Биобрана параллельно с курсом традиционной химиотерапии или таргетной терапии существенно уменьшает число и выраженность осложнений, одновременно на порядок увеличивая эффективность лечения, улучшая прогноз, снижая риск метастазирования и рецидива.